Активность масла тимьяна (Oleum Thymi) против бактерий Acinetobacter baumannii и Pseudomonas aeruginosa, обладающих множественной лекарственной устойчивостью
Вскоре после начала лечения инфекционных заболеваний антибиотиками были отмечены случаи устойчивости к ним бактерий. В настоящее время штаммы бактерий с множественной лекарственной устойчивостью выделяют главным образом в больницах. Это прежде всего неферментирующие грамотрицательные бациллы, которые проявляют как естественную, так и приобретенную трудно устранимую устойчивость к множественным антибиотикам и дезинфицирующим средствам. Открытие новых, эффективных и безопасных веществ, которые предотвращают неблагоприятные инфекции, крайне необходимо для обеспечения альтернативных возможностей терапии. В связи с этим возрастает интерес к лекарственным средствам природного происхождения, в том числе к эфирным маслам. Особенно важно то, что к их компонентам не возникает антибактериальной устойчивости несмотря на то, что они активны против многих бактериальных штаммов. Целью нашего исследования было оценить антибактериальную активность in vitro масла тимьяна против штаммов A. baumannii и P. aeruginosa, обладающих множественной лекарственной устойчивостью при помощи диско-дифузионного метода и метода макроразведения. Штаммы были изолированы от пациентов, госпитализированных в 2013-2014 годах. Антибактериальную активность in vitro масла тимьяна оценивали диско-диффузионным методом. Диаметр зон ингибиции роста для масла в разных концентрациях, применяемых против A. baumannii, составлял от 7 до 44 мм. Масло тимьяна проявляло низкую активность против штаммов P. aeruginosa. В отношении изолятов A. baumannii испытания методом серийных разведений подтвердили высокую активность масла тимьяна, выраженную в значениях минимальной ингибирующей концентрации (МИК) в диапазоне от 0,25 до 2 мкл/мл. Полученные результаты свидетельствуют о необходимости дальнейших исследований антибактериальной активности эфирных масел, особенно против бактерий с множественной лекарственной устойчивостью.
Целебные свойства эфирных масел, продуктов вторичного метаболизма масляных растений известны на протяжении веков. Несмотря на долгую историю их использования, химический состав эфирных масел не анализировали до девятнадцатого века, когда разработка хроматографических методов позволила исследователям исследовать растительные продукты гораздо более подробно, но только методы хроматографии в сочетании с масс-спектрометрией смогли обеспечить более совершенный анализ (1). В химическом отношении масла представляют собой смеси углеводов, спиртов, альдегидов, кетонов, а также эфиров и эфирных производных обоих терпенов (главным образом моно- и сесквитерпенов) и пропилбензола. Конкретный химический состав эфирного масла зависит от вида растения, но соотношения различных компонентов варьируют в зависимости от климата, условий выращивания, стадии вегетации, а также от того, какая часть растения используется (корни, корневища, травы, листья , цветы, фрукты, семена или кора). Богатый состав эфирных масел определяет их чрезвычайно широкий диапазон биологической активности, в том числе активность против бактерий, вирусов и грибов, которая в основном зависит от природы ведущего химического компонента. Эфирные масла, содержащие фенолы (тимол и карвакрол), эвгенол и циннамальдегид, проявляют самую сильную антибактериальную активность. Масла обладают липофильными свойствами, которые позволяют им быстро проникать в клеточную стенку и цитоплазматическую мембрану, что приводит к повреждению клетки. Эфирные масла мешают работе транспортных белков, что приводит к утечке компонентов бактериальных клеток, ингибирует метаболизм водорода и образование АТФ и влияет на цитоплазматические ферменты, что в конечном итоге вызывает лизис клеток (2-4). Вышеупомянутая активность эфирных масел и их основных компонентов имеет значительный терапевтический потенциал при лечении инфекций. Антиоксидантные, иммуностимулирующие и противовоспалительные свойства масел одинаково важны (5).
Выдающимся достижением 20-го века стало открытие антибиотиков, которые произвели революцию в лечении инфекционных заболеваний. К сожалению, вскоре после их введения в клиническую практику стала отмечаться резистентность бактерий к антимикробным агентам. Недавно было подтверждено прогрессирующее повышение лекарственной устойчивости среди патогенных микроорганизмов, что отрицательно сказывается на результатах лечения инфицированных пациентов.
Среди бактериальных штаммов в настоящее время можно выделить следующие группы микроорганизмов со множественной лекарственной устойчивостью: MDR (multidrug-resistant, со множественной лекарственной устойчивостью), XDR (extensively drug-resistant, с широкой лекарственной устойчивостью) и PDR (с устойчивостью ко всем антимикробным агентам). Микроорганизмы со множественной лекарственной устойчивостью чаще всего встречаются в больничной среде, где они могут вызывать серьезные внутрибольничные инфекции, особенно в отделениях интенсивной терапии, ожоговой терапии, хирургических, гематологических и онкологических (6). Это прежде всего неферментирующие грамотрицательные бациллы, принадлежащие к видам Acinetobacter (A.) baumannii или Pseudomonas (P.) aeruginosa. Микроорганизмы, которые могут выжить при низком содержании питательных веществ, заселяют больничную среду, в том числе санитарные объекты, вентиляцию и медицинское оборудование, в основном респираторы, ингаляторы и венозные или мочевые катетеры (7, 8). Они инфицируют операционные раны и ожоги, тогда как в отделениях интенсивной терапии они являются преобладающими видами бактерий, которые вызывают инфекции дыхательной системы и мочевыводящих путей. Их способность образовывать биопленку способствует выживанию и колонизации респираторов и мочевых катетеров (9,10). Резистентность ко многим антибиотикам и дезинфицирующим средствам, в первую очередь приобретенным, но также и к естественным, проявляемая многими патогенами, затрудняет их уничтожение, поэтому поиск новых, эффективных и безопасных веществ, которые предотвращают такого рода инфекции, становится все более актуальным. Следует отметить, что в последнее время предметом растущего интереса стали лекарственные средства природного происхождения, в том числе эфирные масла, к компонентам которых не развивается антибактериальная устойчивость. Не исключено, что использование эфирных масел при лечении инфекций, вызванных микроорганизмами с множественной лекарственной устойчивостью, может стать мощной альтернативой синтетическим антибиотикам, эффективность которых за последнее десятилетие снизилась. В поисках соединений или веществ, которые препятствуют инфекциям или распространению инфекционных агентов в больничной среде, мы изучили влияние тимьянового масла на некоторые штаммы неферментирующих бацилл со множественной лекарственной устройчивостью.
Целью исследования было оценить антибактериальную активность in vitro масла тимьяна (Oleum Thymi) против эталонных штаммов с множественной лекарственной устойчивостью A. baumannii и P. aeruginosa при помощи диско-дифузионного метода и метода макроразведения.
Материалы и методы
Мы исследовали натуральное масло тимьяна, сертифицированное в соответствии со стандартами Национального института гигиены. Исходное 100% масло серийно разбавляли в диметилсульфоксиде (ДМСО) для достижения конечных концентраций 50, 25, 12,5, 6,25 и 3,125%. Были исследованы следующие штаммы A. baumannii: 59 клинических изолятов и эталонный штамм ATCC 19606, а также штаммы P. aeruginosa: 29 клинических изолятов и эталонный штамм ATCC 27853. Штаммы были выделены от больных, госпитализированных в 2013-2014 гг. в специализированную больницу им. Л. Ридигера в Кракове в отделения анестезии и интенсивной терапии, ожоговой терапии, множественной травматологической помощи, ортопедии и нейроортопедии, неврологии и травм головного мозга, пластической хирургии, нефрологии, кардиологии и внутренней медицина, а также токсикологии. Изоляты Acinetobacter baumannii культивировали из эндотрахеальных аспиратов (22 штамма), образцов крови (17), мазков из ран (12), мочи (4) и катетеров (4), тогда как изоляты P. aeruginosa культивировали из мазков из ран (11), эндотрахеальных аспиратов (9), мочи (4), мазков из уха (4) или из конъюнктивы (1). Все исследованные штаммы A. baumannii и P. aeruginosa обладали множественной лекарственной устойчивостью. Испытывали чувствительность изолятов A. baumannii (59) к имипенему (IPM), меропенему (MEM), амикацину (AMK), гентамицину (GEN), тобрамицину (TOB), ципрофлоксацину (CIP), колистину (CST) и триметоприну/сульфаметоксазолу (SXT). Для определения чувствительности штаммов P. aeruginosa (29) использовали следующие антибиотики: пиперациллин (PIP), пиперациллин/тазобактам (TZP), цефтазидим (CAZ), цефепим (FEP), имипенем, меропенем, азтреонам (АТМ), амикацин, гентамицин, тобрамицин, ципрофлоксацин и колистин.
Материалы и методы
Чувствительность штаммов A. baumannii и P. aeruginosa к антимикробным агентам оценивали диско-диффузионным методом и определяли минимальные ингибирующие концентрации (МИК). Полученные результаты свидетельствуют о том, что эти изоляты следует классифицировать как обладающие множественной лекарственной устойчивостью (Рисунки 1 и 2). 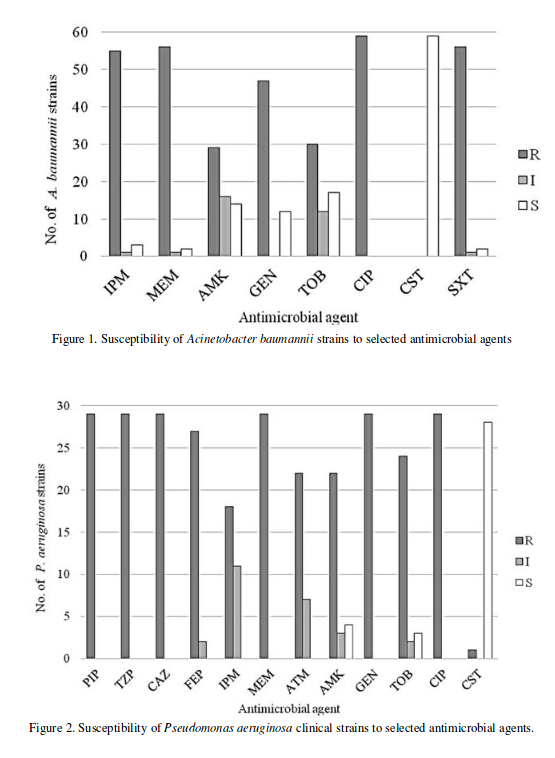
Рисунок 1
Чувствительность штаммов Acinetobacter baumannii к
избранным антимикробным агентам. По горизонтальной оси – антимикробный
агент, по вертикальной оси – количество штаммов.
Рисунок 2
Чувствительность
штаммов Pseudomonas aeruginosa к избранным антимикробным агентам. По
горизонтальной оси – антимикробный агент, по вертикальной оси –
количество штаммов.
Чувствительность штаммов Acinetobacter baumannii к избранным антимикробным агентам
Антибактериальную активность масла тимьяна определяли диско-диффузионным методом и методом серийных разведений для того, чтобы найти минимальную ингибирующую концентрацию, способную тормозить рост бактерий. Изоляты инокулировали на твердую среду (триглицериновый соевый агар) и инкубировали при 35°С в течение 20 часов. Затем колонии суспендировали в 0,85% физиологическом растворе, чтобы получить эквивалент 0,5 единиц МакФарланда по мутности. Тесты на диффузию диска проводились на агаре Мюллера-Хинтона в чашках Петри диаметром 90 мм. Бактериальные суспензии инокулировали на поверхность чашки Петри с питательной средой, а затем на эту поверхность помещали стерильные фильтровальные бумажные диски диаметром 6 мм, содержащие уменьшающиеся концентрации масла тимьяна (15 мкл). После 20 ч инкубации при 35°С измеряли диаметры зон ингибирования роста в мм. Минимальные ингибирующие концентрации определяли методом макроразведения триптиказеино-соевом бульоне.
Объемы были подобраны таким образом, чтобы объем растворителя был как можно меньшим. Исходный раствор получали путем растворения чистого масла тимьяна в ДМСО до концентрации 16 мкл/мл, а затем делали серийные разведения в пределах от 8 мкл/мл до 0,125 мкл/мл в пробирках, содержащих 1 мл бульона. Затем к каждой пробирке добавляли 100 мкл бактериальной суспензии, эквивалентной 0,5 единицам McFarland, и инкубировали при 35°C в течение 20 часов. После этого определяли минимальную ингибирующую концентрацию (МИК, мкг/мл) как самую низкую концентрацию тимьянового масла, при которой не наблюдалось бактериального роста. Параллельно со всеми испытаниями проводили контроль бульона, масла тимьяна и роста бактерий.
Результаты
В настоящем исследовании мы изучали in vitro антимикробную активность масла тимьяна против бактериальных эталонных штаммов. Испытания проводили диско-диффузионным методом и измеряли диаметры зон ингибиции роста бактерий вокруг дисков, пропитанных маслом тимьяна.
.png)
Зоны ингибирования роста клинического штамма Acinetobacter baumannii маслом тимьяна в концентрации: A. 100% масло тимьяна; B. 50% масло тимьяна; C. 25%, 12,5%, 6,25% масло тимьяна. Сравнение чувствительности к 100% маслу тимьяна с устойчивостью к выбранным антибактериальным агентам: IPM, GEN, TOB, CIP, SXT (D)..png)
Значения МИК масла тимьяна (мкл/мл) против клинических штаммов Acinetobacter baumannii. По горизонтальной оси – значения МИК, по вертикальной оси – количество штаммов.
Таблица 1. Диаметры зон ингибиции роста Acinetobacter baumannii (клинические и эталонные штаммы) тимьяновым маслом в тестируемых концентрациях, определенные диско-диффузионным методом
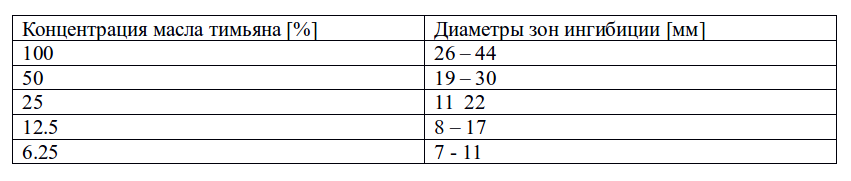
Таблица 2. Диаметры зон ингибиции роста клинических штаммов Pseudomonas aeruginosa strains growth тимьяновым маслом в тестируемых концентрациях, определенные диско-диффузионным методом

Диаметры зон ингибиции для эталонного штамма ATCC 19606 A. baumannii варьировали от 9 до 38 мм при концентрациях масла 100, 50, 25, 12,5 и 6,25%, тогда как при концентрациях масла 100, 50 и 25% зоны ингибирования штамма АТСС 27853 P. aeruginosa составляли от 7 до 18 мм. Те же концентрации были использованы для оценки антибактериальной активности тимьянового масла против патогенов, выделенных из пациентов стационара. Наши результаты подтвердили, что антибактериальная активность масла тимьяна против изученных штаммов A. baumannii была высокой. Размер зон ингибирования составлял от 26 до 44 мм для масла тимьяна в концентрации 100%, от 19 до 30 мм для 50%, от 11 до 22 мм для 25% и от 8 до 17 мм для 12,5%. Наименьшие зоны ингибирования в диапазоне от 7 до 11 мм были получены при концентрации масла 6,25% (таблица 1). Результаты исследования восприимчивости к маслу тимьяна клинического изолята A. baumannii показаны на рисунке 3. Наше исследование показало очень низкий уровень активности тимьянового масла против тестируемых клинических штаммов P.aeruginosa. Масло тимьяна создавало зоны ингибирования роста бактерий в диапазоне от 7 до 12 мм для 11 штаммов P.aeruginosa, но оказалось, что оно полностью неактивно против восемнадцати изолятов этого патогена (таблица 2). Следующим этапом исследования было определение значений МИК масла тимьяна в различных концентрациях против штаммов A. baumannii с использованием метода серийного разведения. Полученные результаты подтвердили, что антибактериальная активность масла тимьяна, выраженная в значениях МИК, составляющих от 0,25 до 2 мкл/мл, была высокой. Было обнаружено, что МИК50 и МИК90 этих изолятов составляют 0,5 и 1 мкл/мл соответственно. Самый низкий МИК 0,25 мкл/мл наблюдался против штамма A. baumannii, в то время как значения 0,5 мкл/мл и 1 мкл/мл были обнаружены у 31 и 17 изолятов, соответственно. Только один штамм показал МИК 2 мкл мл (рисунок 4).
Обсуждение и выводы
В двадцатых годах прошлого века французский химик Рене Гаттефоссе (René Gattefossé ) заинтересовался целебными свойствами эфирных масел после нанесения лавандового масла на ожог на руке. В 1937 году Гаттефоссе придумал слово «ароматерапия» для описания использования эфирных масел в терапии (2). В последнее время интерес к использованию натуральных продуктов в медицине возрастает. Несмотря на то, что новые антимикробные препараты, в основном антибактериальные, появились на рынке, они все еще неэффективны. Существует настоятельная необходимость поиска новых агентов, в том числе натуральных продуктов с высокой антимикробной активностью, не дающих никаких неблагоприятных эффектов. Исследования доказали, что эфирные масла обладают замечательным антимикробным потенциалом и очень эффективны против грамположительных и грамотрицательных бактерий. В нескольких исследованиях было установлено, что эфирные масла могут увеличить бактериальную восприимчивость к лекарствам даже из наиболее устойчивых штаммов (3, 4, 11), поэтому терапия эфирными маслами в сочетании с антибиотиками может не только улучшить результаты лечения, но также замедлить усиление бактериальной резистентности к антибиотикам. Самая сильная антибактериальная активность проявляется эфирными маслами, обогащенными фенолом; одним из них является масло тимьяна, которое получено из травы Thymus vulgaris (12).
Тимол, основной компонент, составляет 30-50% масла тимьяна и карвакрол - до 5%. Эфирное масло тимьяна также содержит ряд дополнительных соединений, таких как терпены, танины, флавоноиды, сапонины и минералы (2). Тимьян действует как отхаркивающее средство, поэтому он используется при заболеваниях дыхательных путей. Благодаря антимикробной и антисептической активности тимьян используется при дезинфекции кожи, лечении себорейного дерматита и бактериальной экземы, а также для ускорения заживления ран. Тимьян также часто используют в ароматерапии и для ухода за кожей: массаж, ванны, ингаляции и очищение лица (2, 13, 14). Результаты наших исследований подтвердили высокую активность масла тимьяна против штаммов A. baumannii со множественной лекарственной устойчивостью, выделенных у пациентов, госпитализированных в различные отделения клиники. Мы получили аналогичные результаты, используя диско-дифузионный метод (диаметры зон ингибирования роста бактерий варьировали от 7 до 44 мм) и метод серийного разведения (МИК от 0,25 до 2 мкл/мл). Наши результаты согласуются с результатами работы Lysakowska и др., которые исследовали бактерии рода Acinetobacter, обладающие множественной лекарственной устойчивостью, выделенные из больничной среды и госпитализированных пациентов. Они определили значения МИК в диапазоне от 0,25 до 1 мкл/мл (15). Hersch-Martinez и др. изучали восприимчивость различных видов бактерий к тимьяновому маслу с использованием диско-диффузионного метода и получили средний диаметр зон ингибиции роста бактерий от 6,4 до 35,7 мм. Для штаммов P. aeruginosa это значение составляло 6,4 мм (16). В нашем исследовании диаметр зоны торможении роста P.aeruginosa не превышал 12 мм, что считается очень низким антибактериальным эффектом. Hammer и др. определяли антимикробную активность 53 эфирных масел, в том числе масла тимьяна, против различных видов бактерий с использованием метода серийных разведений как агара, так и бульона. Минимальные ингибирующие концентрации с маслом тимьяна против эталонного штамма NTCT 7844 A. baumannii составили 0,12 мкл/мл и против P. aeruginosa NTCT 10662 более 2 мкл/мл (17). Kedzia et al. исследовали антимикробную активность тимьянового масла против 31 бактериального штамма различных видов, включая три штамма A. baumannii и один штамм от каждого вида: P. aeruginosa и P. stutzerii. Они использовали серийные разведения масла тимьяна в агаре Мюллера-Хинтона. Установлено, что значения МИК для штаммов A. baumannii варьировали от 0,5 до 2 мг/мл, для P. aeruginosa - более 4 мг/мл, а для P. stutzerii - 0,5 мг/мл (18). Sienkiewicz и Wasiela тестировали 30 штаммов P. aeruginosa с использованием масла тимьяна, предварительно разбавленного в этаноле и затем серийно разведенного в агаре. Значения МИК находились в диапазоне от 1 до 2.5 µL/mL (19). В соответствии с этими выводами мы также продемонстрировали высокую антимикробную активность тимьянового масла против штаммов A. baumannii. Хотя эти результаты обнадеживают, необходимо продолжить исследования по антибактериальной активности эфирных масел, особенно в отношении штаммов клинически значимых видов бактерий со множественной лекарственной устойчивостью. Стоит отметить, что многие продукты, содержащие эфирные масла и рекомендуемые для лечения различных состояний, защищены патентами. Синергическое противомикробное действие эфирных масел и антибактериальных средств не только могло бы помочь искоренить сам источник инфекции, но также могло бы замедлить рост бактерий, резистентных к антибиотикам (20). Современные методы лечения серьезных бактериальных инфекций, вызванных резистентными штаммами, включают комбинированную терапию антибиотиками широкого спектра действия (21). Особое внимание следует уделить колистину, антибиотику из группы полимиксинов, который был вновь введен в клиническую практику для лечения инфекций, вызванных бактериальными штаммами с множественной лекарственной устойчивостью, в том числе A.baumannii and P. aeruginosa (MDR, XDR, PDR). Колистин, хотя и эффективен, дает побочные эффекты и может взаимодействовать с другими лекарствами. Это особенно актуально для пациентов с серьезными сопутствующими заболеваниями. К сожалению, среди чувствительных к колистину больничных изолятов в последнее время появились резистентные к колистину штаммы (22). Длительная антимикробная терапия у госпитализированных пациентов нарушает нормальную флору, способствуя обострению серьезных сопутствующих инфекций. В последние годы изолировано все больше штаммов, обладающих множественной лекарственной устойчивостью, но разработано лишь небольшое количество новых противомикробных препаратов для клинического применения. Поэтому необходимо продолжить исследования новых продуктов, в том числе эфирных масел, поскольку их использование в комбинированной терапии с помощью антибиотиков может быть альтернативной терапией для отдельных инфекций и лучше изучить антибактериальную активности эфирных масел, поскольку бактериальная резистентность к лекарствам постоянно возрастает. Наши результаты показывают, что активность масла тимьяна in vitro против мультирезистентных штаммов A. baumannii высока, что говорит о возможности использования этого масла для лечения инфекционных заболеваний и для уничтожения патогенов в больничной среде.
Литература
1. Kubeczka K.-H.: in Handbook of essential oils: science, technology, and applications, Baser K.H.C., Buchbauer G. Eds., pp. 3-5, CRC Press, Boca Raton 2010.
2. Pisulewska E., Janeczko Z.: Polish oil plants: occurrence, cultivation chemical composition and uses, pp. 7-11, Know-How, Krakow 2008.
3. Yap P.S., Yiap B.C., Ping H.C., Lim S.H.: Open Microbiol. J. 8, 6 (2014).
4. Nazzaro F., Fratianni F., De Martino L., Coppola R., De Feo V.: Pharmaceuticals (Basel) 6, 1451 (2013).
5. Edris A.E.: Phytother. Res. 21, 308 (2007).
6. Fleischer M., Przondo-Mordarska A.:Zakaшenia 2, 30 (2006).
7. Gellatly S.L., Hancock R.E.: Pathog. Dis. 67,159 (2013).
8. Gordon N.C., Wareham D.W.: Int. J.Antimicrob. Agents 35, 219 (2010).
9. Mulcahy L.R., Isabella V.M., Lewis K.:Microb. Ecol. 68, 1 (2014).
10. Longo F., Vuotto C., Donelli G.: NewMicrobiol. 37, 119 (2014).
11. Krol S.K., Skalicka-Wozniak K., Kandefer-Szersze Т.M., Stepulak A.: Postepy Hig. Med. Dosw. (Online) 67, 1000 (2013).
12. Sienkiewicz M., Denys P., Kowalczyk E.: Int.Rev. Allergol. Clin. Immunol. 17, 36 (2011).
13. Nowak G., Nawrot J.: Herba Polonica 55, 178 (2009).
14. Angelucci F.L., Silva V.V., Dal Pizzol C., SpirL.G., Praes C.E., Maibach H.: Int. J. Cosmet.Sci. 36, 117 (2014).
15. Lysakowska M., Denys A., Sienkiewicz M.: Cent. Eur. J. Biol. 6, 405 (2011).
16. Hersch-Martinez P., Leanos-Miranda B.E.,Solorzano-Santos F.: Fitoterapia 76, 453 (2005).
17. Hammer K.A., Carson C.F., Riley T.V.: J. Appl. Microbiol. 86, 985 (1999).
18. Kedzia A., Dera-Tomaszewska B., Ziolkowska-Klinkosz M., Kedzia A.W., Kochanska B., Gebska A.: Postepy fitoterapii 2, 67 (2012).
19. Sienkiewicz M., Wasiela M.: Postepy fitoterapii 3, 139 (2012).
20. Wolska K.I., Grzes K., Kurek A.: Pol. J.Microbiol. 61, 95 (2012).
21. Kowalska-Krochmal B.: Zakazenia 1, 22(2012).
22. Petrosillo N., Ioannidou E., Falagas M.E.: Clin.Microbiol. Infect. 14, 816 (2008).
Источник
Опубликовано: D.Trojanowska, P. Paluchowska, Ј.Sonja, A. Budak. Activity of thyme oil (Oleum thymi) against multidrug-resistant Acinetobacter baumannii and Pseudomonas aeruginosa. Acta Poloniae Pharmaceutica & Drug Research, Vol. 73 No. 4 pp. 975-981, 2016.
Перевод и редактирование: Г.Б.Большакова
Похожие статьи
Клетки людей, страдающих акне, могут быть защищены от старения
Ученые из Королевского колледжа в Лондоне обнаружили, что люди, которые
ранее страдали от акне, по всей видимости, имеют более длинные
теломеры в белых кровяных клетках, то есть их клетки могут быть лучше
защищены от старения.
Даниэль Райман "Использование эфирных масел и растений"
Эфирные масла могут представлять опасность. Автор статьи предостерегает об ошибках и рекомендует наиболее благоприятные методики использования.
Рекомендуемые товары
Теги: ароматерапия, эфирное масло,